חידושים אחרונים בטיפול בסרטן ריאה
סרטן ריאות הוא הגידול הממאיר הנפוץ ביותר ובעבר אבחונו בישר על תמונת מצב עגומה. פיתוחם של טיפולים מתקדמים, ובהם טיפולים ביולוגיים ואימונותרפים, הוביל לשיפור משמעותי בסיכויי ההישרדות מהמחלה, כמו גם באיכות חייהם של החולים בה. כל הפרטים בכתבה
סרטן הריאות מהווה את אחת מהמחלות הממאירות השכיחות ביותר בעולם המערבי והוא נחשב לגורם התמותה המוביל בהשוואה לכלל הגידולים הממאירים הקיימים.
סרטן הריאה היא אינה מחלה אחת, אלא קבוצת מחלות המחולקת לשני סוגים מרכזיים:
סרטן ריאות מסוג תאים קטנים
סוג זה של סרטן ריאות נדיר יותר ומהווה כ-15-20% מכלל הגידולים הממאירים המתפתחים בריאה. התפתחותו לרוב סוערת – הוא גדל במהירות ונוטה לשלוח גרורות לאיברים אחרים. גידול זה נוטה להתפתח בקרב מעשנים או מטופלים שעישנו בעבר.
סרטן ריאות מסוג תאים שאינם קטנים
סוג זה מתפתח בקרב רוב החולים ומהווה כ-80%-85% מכלל הגידולים הממאירים בריאה. מדובר בגידול ייחודי מאחר שהוא עלול להתפתח בקרב מעשנים פעילים, מטופלים שעישנו בעבר וכן גם בקרב אנשים שמעולם לא עישנו.
סרטן ריאות מסוג תאים שאינם קטנים נחלק למספר תתי קבוצות בהתאם למקור התאי שממנו החל הגידול להתפתח:
- סרטן של תאים קשקשים ((squamous cell carcinoma – מקורו הוא בצינורות הנשימה החיוניים. סוג זה מהווה כרבע מהגידולים הסרטניים מסוג תאים שאינם קטנים המתפתחים בריאה.
- אדינוקרצינומה (Adenocarcinoma) – הסוג הנפוץ ביותר של סרטן ריאה מסוג תאים שאינם קטנים. מקורו הוא באזור שבו מתקיימים חילופי הגז בריאות.
- סרטן של התאים הגדולים (large cell carcinoma) – סוג זה מאופיין גם הוא בהתפתחות מהירה.
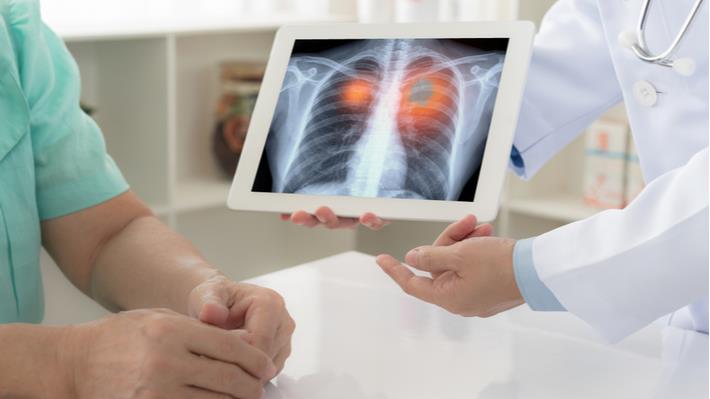
create jobs 51 | Shutterstock
לצד עישון, מהם גורמי הסיכון שעלולים להוביל להתפתחות של סרטן ריאה מסוג תאים שאינם קטנים?
עישון מהווה אמנם את גורם הסיכון המרכזי להתפתחות של סרטן מסוג זה, והוא נוכח בכ-90% מכלל המקרים. לצד זאת, ישנם גורמי סיכון נוספים המעלים את הסיכוי להתפתחות של הגידול הממאיר, ובהם קיום של מחלת ריאות חסימתית כרונית וכן גם חשיפה לחומרים שונים כדוגמת אסבסט, סולר, גז רדון וקרינה מייננת.
מהן אפשרויות הטיפול במחלה?
הטיפול במחלה משתנה ממטופל/ת למטופל/ת ותלוי בגורמים שונים, בהם גם שלב המחלה. בשלב 1 הטיפול לרוב יכלול ניתוח להסרת הגידול הממאיר והוצאה של שוליים בריאים. בשלבים מתקדמים יותר, קיים כיום ארסנל טיפולי רחב הכולל כימותרפיה, טיפול בקרינה וכן גם טיפולים אימונותרפים ביולוגיים.
טיפולי העבר בסרטן הריאה
בשלבים הראשונים להתפתחות הגידול (שלב 1-2) החלופה הטיפולית העדיפה הייתה ניתוחית ונותרה כך עד היום. עם זאת, בשלבים 3-4 החלופות הטיפוליות היו אחרות מאלה הקיימות כיום ויעילותן הייתה פחותה: לחולים בשלב 3, החלופה העדיפה כללה מתן של טיפול כימותרפי, קרינה והמשך מעקב. בקרב חולים בשלב 4 ניתן טיפול כימותרפי בלבד ועם התקדמות המחלה בוצע שינוי בתרופה הכימותרפית שניתנה.
מה הסיכוי לחזרת המחלה לאחר טיפול בגידול הראשוני?
הסיכוי לחזרת המחלה תלוי גם הוא בצירוף של גורמים ונגזר בחלקו גם משלב המחלה בעת האבחון. בשלב 1, הסיכוי לחזרת המחלה נמוך יחסית ועומד על 5-10%. שיעור ההישרדות בקרב חולים שאובחנו בשלב זה גבוה מ-90% במעקב של חמש שנים.
בשלב 2 הסיכוי לחזרת המחלה לאחר ביצוע של ניתוח עומד על כ-30% ושיעור ההישרדות במעקב של חמש שנים הוא כ-70%.
בקרב מטופלים בשלב 3 ו-4, החידושים בטיפול במחלה שיפרו את סיכויי ההישרדות באופן משמעותי. כיום סיכויי ההישרדות של חולים המאובחנים עם גידול בשלב 3 ומטופלים באמצעות כימותרפיה, קרינה וטיפול אימונותרפי עומדים על כ-35%-40% במעקב של ארבע שנים. באשר לחולים בשלב 4 הסובלים ממחלה גרורתית, נכון לכתיבת שורות אלה שיעורי ההישרדות חוצים את השנתיים בחלק מהמקרים.
חשוב לציין כי מטופלים עם רקע של עישון, נמצאים בסיכון גבוה יותר לחזרת מחלה (בשלבים מוקדמים: 1-2). בנוסף, מחקרים הוכיחו כי בקרב מטופלים שאינם מעשנים, ישנה תגובה טובה יותר לטיפול אונקולוגי.
שיפור באיכות החיים ובסיכויי ההישרדות: הטיפולים החדשים בסרטן הריאה
הרפואה המודרנית הביאה הובילה להתפתחות ניכרת בתחום האונקולוגיה ככלל, וטיפול בסרטן הריאות בפרט. כיום קיים ארסנל טיפולי רחב בסרטן ריאות מסוג תאים שאינם קטנים, בייחוד בשלבי מחלה מתקדמים. גידול זה מאופיין בהימצאות של מוטציות רבות, דבר המסייע בהתאמה אישית של הטיפול לכל מטופל ובכך מוביל לשיפור משמעותי של איכות החיים וסיכויי ההישרדות.
שתיים מאפשרויות הטיפול המתקדמות ביותר, הניתנות לרוב לחולים בשלב 3 ו-4, הן טיפול ביולוגי ואימונותרפיה.
טיפולים ביולוגים הם טיפולים מכווני מטרה אשר מזהים את המנגנון בגידול האמון על התפתחותו ופועלים כנגדו.
טיפול אימונותרפי משפיע על מערכת החיסון של הגוף. למעשה, בקרב אנשים בריאים, למערכת החיסון יש יכולת לזהות תאים ממאירים ולפעול כנגדם.
כאשר מתפתח גידול ממאיר, מנגנון ההיכרות של תאי החיסון עם התאים הממאירים משתבש והאחרונים "חומקים" מתגובת מערכת החיסון כנגדם. טיפול אימונותרפי מוריד את השפעתם של גורמים שונים המעכבים את מערכת החיסון של הגוף ועל ידי כך "רותם" את המערכת החיונית לטובת תקיפה של הגידול הסרטני.
כיצד הטיפולים החדשים משפרים את הסיכוי לנסיגת המחלה, מאריכים את ההישרדות ומשפרים את איכות החיים?
הטיפולים החדשניים הובילו לעלייה בשיעורי התגובה לטיפול, כמו גם בסיכויי ההישרדות בקרב חולים שמחלתם מתקדמת. כך לדוגמה, בקרב חולי סרטן ריאה מסוג תאים שאינם קטנים בשלב 4, ניתנת כיום תוספת של משלב טיפול אימונותרפי המשפרת את הסיכוי לנסיגת המחלה. טיפול חדשני זה הוביל לעלייה משמעותית בשיעור הישרדות החולים ובמקרים מסוימים, ישנם מטופלים שעוברים את הרף ללא כל עדות למחלה פעילה או עם קיום של מחלה גרורתית בשליטה.
המשלב האימונותרפי יעיל במיוחד במצבים שבהם התפתחו גרורות מוחיות הנחשבים למורכבים יותר לטיפול. בקרב חולים אלה, השילוב בין טיפול כימותרפי לבין המשלב האימונותרפי הוביל לשליטה טובה יותר בגרורות המוחיות, בייחוד בקרב מטופלים שבהם לא נמצאה מוטציה טיפולית. לצד זאת, הטיפול הוביל גם לעלייה ניכרת בשיעורי ההישרדות.
מה לגבי תופעות הלוואי של התרופות האימונותרפיות?
ייחודן של התרופות האימונותרפיות אינו נעוץ רק בשיפור התגובה לטיפול ובסיכויי ההישרדות, אלא גם בשמירה על איכות החיים של המטופלים במהלך הטיפול. תרופות אלה מאופיינות ברעילות נמוכה יותר ולכן גורמות לפחות תופעות לוואי. הטיפול האימונותרפי מסייע בשמירה על איכות החיים והתופעות שמתפתחות בעקבותיו נסבלות למדי, חלקן אף אינן מורגשות כלל ויזהו בבדיקות הדם בלבד.
לסיכום, מחקרים רבים הוכיחו כי מתן תוספת של המשלב האימונותרפי אל מול טיפול בכימותרפיה בלבד הוביל לשיעורי הישרדות גבוהים יותר ולשיפור משמעותי באיכות חייהם של החולים. לצד הנתונים המחקריים, אנו עדים לשינויים אלה בשטח ונוכחים לדעת כי הטיפול החדשני מסייע למטופלים להמשיך בשגרת חיים למרות המחלה ומסייע בהארכת החיים.

האם המאמר עניין אותך?









 חיפוש רופאים
חיפוש רופאים
 בדיקות
בדיקות
 מונחים
מונחים
 כתבות ומחקרים
כתבות ומחקרים
 ערוצי תוכן
ערוצי תוכן
 מחשבונים
מחשבונים